Опубликованы результаты доклинических испытаний препарата ML7, предназначенного для лечения болезней наружной оболочки глаз
Компания Neuroptis Biotech, специализирующаяся на разработке и исследовании лекарств в области офтальмологии, объявила о положительных результатах доклинических испытаний глазных капель на основе препарата ML7. ML7 предназначен для лечения заболеваний наружной оболочки и придаточного аппарата глазного яблока, в частности - синдрома сухого глаза.
Тестируемая молекула ML7 является первой в ряду новых терапевтических препаратов подобного класса. Она обладает потенциалом вызывать эффективную и целенаправленную терапевтическую реакцию у миллионов людей, страдающих синдромом сухого глаза. Это заболевание повреждает слезный аппарат, что проявляется недостаточным количеством или качеством слезной жидкости и ощущением сухости глаз.
Такой синдром может возникать как без видимой причины (идиопатический), так и в связи с аллергией, воспалением переднего отрезка глаза или с синдромом Гужеро-Шегрена. Он может проявиться также и после катарактальной операции.
Исследования, проведенные на животных, показали отличную переносимость препарата, а также его низкую системную впитываемость (менее одного процента) и превосходную эффективность по сравнению с плацебо, содержавшим те же глазные капли, но без вещества ML7. В доклинических испытаниях ML7.использовался в форме стабильных глазных капель однократной дозировки, не содержащих консервантов.
Результаты доклинических испытаний опубликованы в медицинском журнале IOVS (Investigative Ophthalmology and Visual Science).
«Завершение доклинической работы и испытаний ознаменовало кульминацию усилий команды компании Neuroptis Biotech и её партнеров - компаний Provence Technologies, Octalia, Cerep и Iris Pharma, - сказал генеральный директор компании Neuroptis Biotech, доктор Эрик Бело (Eric Belot). - Мы приступим к первой и второй фазам испытаний через несколько месяцев, как только Европейское ведомство по контролю за медикаментами выдаст разрешение на проведение испытаний на людях».
Материал подготовлен: Theochem
С.В.Савина. доцент кафедры "Морфология, патология животных и биология", кандидат ветеринарных наук
Определение острой токсичности средства «Клиодезив» (1-й этап)
Цель исследований: Определить острую токсичность средства «Клиодезив».
Задачи: 1) Провести оценку ингаляционной опасности средства «Клиодезив».
2) Определить оптимальную дозу средства.
3) Изучить общетоксическое и специфическое действие средства.
Материалы и методы:
Исследования по определению острой токсичности средства «Клиодезив»: проводились на кафедре «Морфология, патология животных и биология» и на базе вивария при ФГБОУ ВПО «Саратовский ГАУ» с 10 ноября 2014 г. по 10 января 2015 г. (ОПП №1 - 10 мг йода/м 3. ОПП №2 – 20 мг йода/м3).
Средство, предназначенное для исследования, представлено в форме порошка от светло - до тёмно – коричневого цвета, с характерным запахом йода. Действующее вещество – йод кристаллический – 40%, вспомогательные вещества – калий азотнокислый – 40% и углеводы (сахар, крахмал или декстрин) до 100%.
Средство "Клиодезив", согласно утверждённой инструкции, может использоваться в виде фумигационного аэрозоля, а также для лечения респираторных болезней с/х животных и птицы, санации воздуха помещений в присутствии животных и дезинфекции объектов ветеринарного надзора.
Все исследования проведены в соответствии с Методическими указаниями МУ 1.2.1105-02 1.2. Общие вопросы. Гигиена, токсикология, санитария. "Оценка токсичности и опасности дезинфицирующих средств" (утв. Главным государственным санитарным врачом РФ 10 февраля 2002 г.)
Для проведения испытаний взята максимально возможная доза средства «Клиодезив».
Исследования:
1) Оценку ингаляционной опасности средства «Клиодезив» проводили в насыщающих концентрациях, в герметичной емкости (в эксикаторе), в которой были созданы условия свободного испарения летучих компонентов средства при комнатной температуре в течение 2-х суток.
2) Испытания проводили на белых нелинейных половозрелых мышах (самцы, масса 20-30 г.), прошедших карантин в течение 14 дней, из расчета объема воздуха на одно животное в час – 2 литра.
3) Дозу испытывали на группе из 4 животных (эксикатор объемом 8 л). Экспозиция составила 2 часа.
4) В ходе эксперимента фиксировали наличие/отсутствие клинических признаков отравления (при наличии - время их появления), а также общее состояние (гибель) животных.
5) После окончания воздействия на животных средства «Клиодезив», проводили обследования по показателям общетоксического и специфического действия препарата. Опасность ингаляционного отравления характеризуется степенью проявления интоксикации. Данные представлены в таблице 1.
Таблица 1 Классификация химических веществ по степени летучести (С20)
22 апреля, 2015 - 05:00
Учеными Алтайского государственного медицинского университета разработан новый препарат под названием «Антилитал», который, по их словам, является сверхэффективным лекарством от мочекаменной болезни. Авторами разработки являются заведующий кафедрой фармакологии АГМУ доктор медицинских наук, профессор Валерий Брюханов, декан фармацевтического факультета АГМУ доктор биологических наук, профессор Вячеслав Лампатов и доктор биологических наук, профессор кафедры фармакологии Александр Жариков.
По словам Вячеслава Лампатова, еще пять лет назад ученые актуализировали гипотезу, родившуюся еще в 80-х годах прошлого века, что ткань мочевых путей и почек одного из биологических видов имеет некий защитный механизм, предотвращающий образование камней. Поэтому данные ткани были использованы для создания препарата, способного лечить мочекаменную болезнь у тех, кто такого защитного механизма не имеет.
Как отметил Александр Жариков, собственных медикаментов, которые успешно, качественно, радикально лечили и предотвращали рецидивы мочекаменной болезни, будучи при этом безопасными для пациента, в России нет. Тем не менее, по статистике, ежегодно мочекаменной болезнью в мире заболевает 10–15 % людей, из них — 15 миллионов человек в России.
По мнению разработчиков, препарат «Антилитал» не имеет аналогов в мире. Уверенность ученого подкреплена данными многолетних доклинических исследований в лаборатории фармакологического факультета АГМУ. Так, в ходе сравнения результатов экспериментов на животных выяснилось, что количество камней после курса препарата уменьшается в 12,5 раз, а их размер — в 3,5 раза. Также доклинические исследования препарата доказывают, что он не имеет побочных эффектов.
На данный момент проект проходит заключительные этапы доклинических испытаний и постепенно готовится к переходу на этап клинических испытаний, требующий экспериментального оснащения и производственной базы. Результаты проводимых доклинических испытаний превосходят самые оптимистические прогнозы ученых АГМУ, у которых появилась обоснованная надежда на прорыв в области лечения и профилактики мочекаменной болезни.
Просмотров: полная версия сайта: 578, Uro+: 33, Мобильная версия сайта: 30

Источники:
, ,
Следующие статьи
- Открыты стволовые клетки, способные помочь лечить слепоту
- Первоначальные результаты клинических исследований коррекции миопии методом ReLEx smile
- По зрительному нерву можно определить риск смерти от инсульта
Комментариев пока нет!
Поделитесь своим мнением

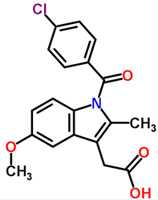 Индометацин
Индометацин  Как лечат глаза в Израиле
Как лечат глаза в Израиле  Сколько стоит операция катаракта глаза в москве
Сколько стоит операция катаракта глаза в москве  Операция катаракта послеоперационный период
Операция катаракта послеоперационный период